Na3Zr2Si2PO12 Naイオン電池用セラミック電解質
Na3Zr2Si2PO12セラミック Naイオン電池用電解質:スプレードライ法による調製とその方法 プロパティ
著者李文凱、趙寧、BI志傑、郭祥新。 Na3Zr2Si2PO12 Naイオン電池用セラミック電解質: を使用した調製 噴霧乾燥法とその性質 無機材料ジャーナル、2022、37(2): 189-196 DOI:10.15541/jim20210486
要約
Naイオン電池は現在、可燃性および爆発性の有機物を使用しています。 電解質、高性能ナトリウムイオン固体の開発が急務となっている より安全で実用的な用途を実現する電解液。 Na3Zr2Si2PO12 はその 1 つです。 広い電気化学ウィンドウを備えた最も有望な固体ナトリウム電解質、 高い機械的強度、優れた空気安定性、および高いイオン伝導性。 しかし、セラミック粒子とバインダーが不均一に混合されるため、 グリーンボディ内の細孔が非常に多いため、高密度を得ることが困難になります。 焼結後の高導電性セラミック電解質。ここでスプレーとは、 Na3Zr2Si2PO12粒子を有効にするために乾燥法が使用されました バインダーで均一にコーティングし、球状の二次粒子に造粒します。の 調製されたままの状態で正規分布した粒子は効果的に相互に接触し、 セラミックグリーンボディの気孔率を低減します。焼結後、Na3Zr2Si2PO12セラミック 噴霧乾燥によるペレットは 97.5% の相対密度を示します 室内でのイオン伝導率は 6.96×10-4 Sâcm-1 温度。対照的に、相対密度と室温 Na3Zr2Si2PO12セラミックペレットのイオン伝導率 噴霧乾燥なしで調製されたものは、それぞれ 88.1% と 4.94×10-4 S×cm-1 にすぎません。[19]
キーワード固体電解質; 噴霧乾燥法。 密度; イオン伝導率; Na3Zr2Si2PO12
ナトリウムイオンとリチウムイオンは両方とも属します 最初のメイングループは、同様の化学的性質とインターカレーションを持っています メカニズムがあり、資源が豊富にあります。そこで、ナトリウムイオン電池は、 リチウムイオン電池を補完できます [1、2、3]。ナトリウムイオン電池が入っている 可燃性で揮発性の有機電解質は安全性に懸念があり、制限されています エネルギー密度。液体電解質の代わりに固体電解質を使用すると、 安全性の問題は解決されることが期待されています[4、5、6、7、8]。無機固体電解質 広い電気化学窓を持ち、高電圧陰極とのマッチングが可能 材料を使用し、それによって電池のエネルギー密度が増加します[9]。しかし、 固体電解質は、低いイオン伝導率や困難などの課題に直面しています。 電極と電解質の間の界面でのイオン透過。その間 界面を最適化するには、まず固体電解質を見つける必要があります。 高いイオン伝導率 [10、11、12]。
現在、最も研究されているのはナトリウムイオンです。 無機固体電解質には主に Na-βâ-Al2O3、NASICON タイプが含まれます。 硫化物。中でもNASICON(Sodium Super Ion Conductors)型高速イオン 導体は全固体ナトリウムイオン電池用途において大きな可能性を秘めています 広い電気化学ウィンドウ、高い機械的強度、安定性により 空気に対して伝導性が高く、イオン伝導性が高い [13,14] 。最初に報告されたのは、 グッドイナフとホンら。 [15、16]。一般式は Na1+xZr2SixP3-xO12 です。 (0≠x≠3)、NaZr2(PO4)3 によって形成される連続固溶体です。 Na4Zr2(SiO4)3 であり、開いた三次元 Na+ 透過チャネルを持っています。 Na1+xZr2SixP3-xO12 には、菱形構造 (R-3c) と単斜晶構造の 2 つの構造があります。 構造 (C2/c、1.8 x 2.2)。 x=2 の場合、Na3Zr2Si2PO12 が最もイオン性が高くなります。 導電性。 300 °C で、Na3Zr2Si2PO12 のイオン伝導率は、Na-βâ-Al2O3 (0.1~) のイオン伝導率に近い 0.2 Sâcm-1 に達することができます。 0.3 Sâcm-1) [15]。現在の室温イオン 文献 [17,18] で報告されている Na3Zr2Si2PO12 の導電率は、 約 ~10-4 Sâcm-1。元素ドーピング イオン伝導性を向上させるために、一般的に次のような方法が使用されます。ナシコンソリッド以来 電解質はオープンスケルトン構造を持っており、さまざまな物質をドープできます。 要素。たとえば、Zr4+ を置き換える元素には、Mg2+、Zn2+、Al3+、Sc3+、 Y3+、La3+、Ti4+、Hf4+、Nb5+、Ta5+など[17、18、19、20、21、22]。それらの P5+ の代替には、Ge5+ および As5+ が含まれます [22]。元素ドーピングに加えて、 Na3Zr2Si2PO12セラミックシートの密度を高めることも一般的な方法です イオン伝導性を向上させるためです。最近、ヤンら。 [18]使用要素 ドーピングと酸素雰囲気中での焼結を組み合わせて高度に合成 濃厚な Na3.2+2xZr2-x ZnxSi2.2P0.8O12 (0≠x≠0.15)。 x=0.1のとき、部屋は 温度でイオン伝導率が最大値(5.27×10-3 S×cm-1)に達します。 Na3Zr2Si2PO12セラミック電解質の調製方法 含まれるもの: 従来焼結 (CS)、液相焼結 (LPS)、スパーク プラズマ焼結 (SPS)、マイクロ波焼結 (MWS)、冷間焼結プロセス (CSP)[18-21、23-29]。その中で、Huang らは、 [20] 従来の焼結を使用 Ga3+をドーピングしてセラミックスの密度を高める方法。セラミック 室温でのイオン伝導率が高く(1.06×10-3 S・cm-1)、電子伝導度が低い(6.17×10-8 S・cm-1)電解質が得られました。張ら。 [21]従来の焼結を採用 カチオンLa3+を導入する方法。中間相Na3La(PO4)2が形成される 粒界にあるNa3.3Zr1.7La0.3Si2PO12セラミックシート 99.6%もの高い濃度が得られます。対応する室温イオン 導電率は 3.4×10-3 Sâcm-1 に達します。王ら。 [23]中古品 高密度のNa3Zr2Si2PO12セラミックスを得るマイクロ波焼結(MWS) 850℃の低い焼結温度で96%の焼結を実現し、0.5時間保持するだけで焼結を軽減 費用がかかります。相対密度 (rrelative)、イオン伝導率 (Ït)、および さまざまな方法で調製されたセラミック電解質の活性化エネルギー (Ea) 表 1 にリストされています。
表 1 NASICON タイプの主要パラメータ 各種焼結法に対応した材料
|
焼結方法 |
構成 |
焼結 |
焼結 |
時間/時間 |
相対/% |
st/(Sâcm-1) |
Ea/eV |
参照 |
|
CSP |
Na3.256Mg0.128Zr1.872Si2PO12 |
140 |
なし |
1 |
82.9 |
0.41×10-4 |
- |
[19] |
|
FH-CSP |
Na3Zr2Si2PO12 |
375 |
NaOH |
3 |
93 |
2.2×10-4 |
0.32 |
[24] |
|
LPS |
Na3Zr2Si2PO12 |
1150 |
NaF |
24 |
- |
1.7×10-3 |
0.28 |
[25] |
|
LPS |
Na3Zr2Si2PO12 |
900 |
Na3BO3 |
10 |
93 |
1.4×10-3 |
- |
[26] |
|
LPS |
Na3Zr2Si2PO12 |
1175 |
Na3SiO3 |
10 |
93 |
1.45×10-3 |
- |
[27] |
|
SPS |
Na3.4Zr1.6Sc0.4Si2PO12 |
1100 |
コハック |
0.1 |
95 |
9.3×10-4 |
- |
[28] |
|
SPS |
Na3Zr2Si2PO12 |
1210 |
なし |
0.5 |
97.0 |
1.7×10-3 |
0.28 |
[29] |
|
MWS |
Na3Zr2Si2PO12 |
850 |
なし |
0.5 |
96 |
2.5×10-4 |
0.31 |
[23] |
|
CS |
Na3Zr2Si2PO12 |
1250 |
なし |
16 |
71.4 |
1.7×10-4 |
0.36 |
[20] |
|
CS |
Na3.1Zr1.9Ga0.1Si2PO12 |
1250 |
なし |
16 |
86.5 |
1.06×10-3 |
0.29 |
[20] |
|
CS |
Na3Zr2Si2PO12 |
1200 |
なし |
24 |
87.6 |
6.7×10-4 |
0.353 |
[21] |
|
CS |
Na3.3Zr1.7La0.3Si2PO12 |
1200 |
なし |
24 |
99.6 |
3.4×10-3 |
0.291 |
[21] |
|
CS |
Na3Zr2Si2PO12 |
1250 |
なし |
- |
84.02 |
2.17×10-4 |
0.407 |
[18] |
|
O2-CS |
Na3.4Zr1.9Zn0.1Si2.2P0.8O12 |
1250 |
なし |
- |
99.46 |
5.27×10-3 |
0.285 |
[18] |
|
CS |
Na3Zr2Si2PO12 |
1250 |
なし |
6 |
88.1 |
4.94×10-4 |
0.34 |
この作品 |
|
SD-CS |
Na3Zr2Si2PO12 |
1250 |
なし |
6 |
97.5 |
6.96×10-4 |
0.32 |
この作品 |
CS: 従来の焼結。 SD: 噴霧乾燥。 O2-CS: 従来の純粋な焼結 酸素; CSP: 冷間焼結プロセス; FH-CSP: 溶融水酸化物冷間焼結 プロセス; MWS: マイクロ波焼結。 LPS: 液相焼結。 SPS: スパーク プラズマ焼結
従来の方法では、次のように調製された粉末が使用されます。 直接焼結してバインダーと混合してセラミック素体粉末を生成し、 粉末成形と高温焼結を経てセラミックスが得られます [30, 31、32]。しかし、粉砕・混合の過程で、混合が不均一になるため、 バインダーとセラミック粒子の接触不良や粒子間の接触不良が発生します。 素地内部には気孔が多く、セラミックの作製が困難 高密度でイオン伝導性の高い電解質。スプレードライというのは、 アトマイザーを使用してスラリーを液滴に分散させて急速乾燥させる方法 熱風を使用して液滴を乾燥させ、粉末を取得します。の粒子 噴霧乾燥により製造された粉末は球状であり、バインダーが均一に分散されます。 粒子の表面にコーティングされている[33]。 KOUら[34] スプレードライを使用 高温焼結と組み合わせて固体電解質を合成 高温イオン性の Li1.3Al0.3Ti1.7SixP5(3-0.8x)O12 (LATSP) 導電性。 x=0.05 の場合、室温でのイオン伝導率は a に達します。 最大 1.053 × 10-4 Sâcm-1、圧縮された 密度は 2.892 gâcm-3 で、理論密度に近い 2.94g·cm-3のLATSP。噴霧乾燥により、 セラミックの密度とイオン伝導性の向上における特定の利点 電解質。噴霧乾燥の利点を考慮すると、元素の効果は セラミックの密度とイオン伝導性のドーピングを考慮する必要があります。これ 研究はNa3Zr2Si2PO12を研究対象として選択し、スプレーを導入しました 造粒法を粉末材料の下準備に加えて、 高密度かつ高イオン性のNa3Zr2Si2PO12セラミック電解質を準備します 導電率。
1 実験方法
1.1 材料の準備
Na3Zr2Si2PO12粉末の調製方法: Na2CO3 (アラジン、99.99%)、NH4H2PO4 (アラジン、99%)、ZrO2 (アラジン、99%) の重量を量ります。 化学量論比によると、SiO2 (Aladdin、99.99%)。で 焼結中のNaとPの揮発を補うため このプロセスでは、原料には 8% 過剰の Na2CO3 と 15% 過剰の Na2CO3 が含まれています。 NH4H2PO4 [25]。ボールミル媒体としてジルコニアボールを使用しました。 材料とボールの重量比は 1:3、無水エタノールを分散液として使用しました。 ボールミルを12時間ボールミル粉砕に使用した。ボールミル加工された スラリーをオーブン中80℃で12時間乾燥させた。乾燥させた粉末を粉砕し、 150 メッシュ (100 μm) のふるいを通過させた後、400 °C の濾過器に移した アルミナるつぼで2時間放置。前駆体から CO32- と NH4+ を除去し、加熱します。 1000~1150℃で焼成し、12時間後にアニールして得ます。 Na3Zr2Si2PO12粉末。
Na3Zr2Si2PO12セラミックスの作製方法 シート: Na3Zr2Si2PO12 粒子サイズがシートに及ぼす影響を調査するため、 セラミックシートの密度に応じて、2 セットの対照実験を設計しました。の 最初のグループは従来の方法を使用し、2% (質量分率) のポリビニルを添加しました。 純粋相Na3Zr2Si2PO12粉末にアルコール(アラジン、Mw~205000)結合剤を添加 無水エタノールで混合し、12 時間ボールミル粉砕します。ボールミル粉砕後の粉末は、 乾燥、粉砕、篩にかけて、粒子上に結合剤でコーティングされた粉末を得る 表面。粉末はステンレスを使用して 200 MPa で一軸冷間プレスされます。 スチール金型を使用して Ï12 mm のグリーン ボディを作成し、GB として記録されます。 。減らすために セラミックシートの焼結プロセス中のNaとPの揮発、 グリーン体を母粉中に埋め込み、1250℃で6時間焼結した。 時間後、4℃/分の加熱速度でアニールします。得られたもの Na3Zr2Si2PO12 セラミック電解質は CS-NZSP と呼ばれます。 2番目のグループ は、噴霧乾燥機 (ADL311S、ヤマト、日本) を使用して Na3Zr2Si2PO12 粉末を造粒しました。 2% (質量分率) のポリビニル アルコール (アラジン、分子量 ~205000) バインダーと 2% を追加します。 Na3Zr2Si2PO12粉末へのポリエチレングリコール(アラジン、Mn=1000)分散剤、 そして無水エタノールを加えます。固形分15質量%の懸濁液を調製する フラクションとボールミルで 12 時間処理します。ボールミル粉砕した懸濁液を噴霧乾燥した 入口温度 130 °C、供給流量 5 mL/min。の Na3Zr2Si2PO12粉末をサイクロン分離器を通して収集した。打錠 セラミックの焼結プロセスは最初のグループと同じであり、 得られたNa3Zr2Si2PO12グリーン体とセラミック電解質を次のように記録した。 それぞれ SD-GB と SD-CS-NZSP。セラミックの表面研磨処理 タイル: 最初に 400 メッシュ (38 μm) のサンディング ペーパーを使用して粗研磨し、次に 1200 メッシュ (2.1 μm) のサンディング ペーパーを使用して、セラミックが表面になるまで細かく研磨します。 表面は滑らかです。 CS-NZSP および SD-CS-NZSP セラミック電解質の直径 シートはそれぞれ (11.3±0.1) と (10.3±0.1) mm、厚さは (1.0±0.1)mm.
1.2 材料の物理的特性評価
サンプルの相分析は次のとおりです。 X線回折装置(XRD、Bruker、D8 Advance)を使用して実施した。の 放射線源は CuKα、管圧力は 40 kV、管流量は 40 mA、 スキャン速度は 2 (°)/min、スキャン範囲は 2θ= 10°~80° です。走査 電子顕微鏡(SEM、日立製、S-4800)および透過型電子顕微鏡 (TEM、日本電子、JEM-2100F) を使用してサンプルの形態を分析し、 構成された EDX アクセサリは元素分析に使用されました。
1.3 電気伝導度の測定 セラミックシート
電気化学インピーダンス分光法 電気化学ワークステーションを使用してサンプルの (EIS) をテストしました。テスト 周波数範囲は7 MHz〜0.1 Hz、印加電圧は10 mV、テスト曲線 が取り付けられ、セラミック片のイオン伝導率は以下を使用して計算されます。 式(1).
Ï=L/(RÃS) (1)
式中、L は厚さです。 セラミックシート (cm)、R は抵抗 (Σ)、S は遮断電極面積 (cm2)、Ï はイオン伝導率 (Sâcm-1) です。
サンプルの電子伝導率 直流分極 (DC)、定電圧 5 を使用してテストされました。 V、持続時間は 5000 秒。曲線が安定した後の縦座標値 は分極電流値です。式 (2、3) を使用して、 セラミックシートの電子伝導性とナトリウムイオン移動数。
Ïe=LÃI/(VÃS) (2)
t=(Ï-Ïe)/Ï (3)
式中、L は厚さです。 セラミックシート (cm)、I は分極電流 (A)、V は電圧 (V)、S はブロッキング電極面積 (cm2)、Ïe は電子伝導率 (S∙cm-1) です。この作品ではブロッキング電極として Au を使用しています。の準備 ブロッキング電極:高真空耐性蒸着装置を使用 (VZZ-300) 蒸発源のAuを抵抗加熱により蒸発させ、 セラミックシートの表面に蒸着させます。セラミックシートは、 内径8mmのフェルールに固定されています。
2 結果と考察
2.1 相構造と形態 Na3Zr2Si2PO12の特性評価
焼結を最適化するために Na3Zr2Si2PO12の温度で、粉末を1000、1050、1100、および1100℃で焼結した。 それぞれ1150€。得られたサンプルのX線回折パターン 異なる温度での焼結を図 1 に示します。 図より、焼結温度が1000℃の場合、主相が Na3Zr2Si2PO12 が生成されていますが、Na2ZrSi2O7 と ZrO2 の不純物が存在します。 主相の回折ピーク強度は弱く、 半値幅が広く、焼結品の品質が悪いことがわかります。 結晶性。焼結温度が1100℃の場合、ZrO2不純物が 相が消失し、Na2ZrSi2O7不純物の回折ピーク強度が減少 相が弱くなり、焼結温度を上げると、 不純物相の除去に有益です。の回折ピークは、 1100 および 1150 °C で焼結した製品は、半値幅がより小さくなります。 1000 ℃で焼結した製品の回折ピークは、 焼結温度が高いほど、製品の結晶化度は良くなります。 1000Åの焼結品に比べ、1150Åの焼結品は回折ピークが大きくなっています。 焼結品は2θ = 19.2°、27.5°、30.5°で分割されます。これは、 材料は、イオン伝導率の低い菱形相から、 高いイオン伝導率を持つ単斜晶相 [25,35]。そして回折ピーク 標準 PDF 84-1200 回折ピークと一致しており、次のことを示しています。 1150℃はNa3Zr2Si2PO12固体電解質の相形成温度です イオン伝導性の高い単斜晶構造を持っています。
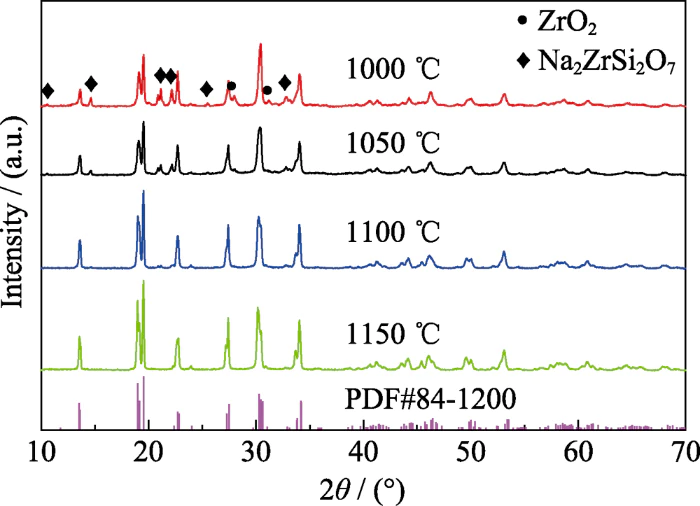
図。 1 XRD Na3Zr2Si2PO12粉末焼結のパターン 異なる温度で
図2にSEM写真とTEM写真を示します。 従来の混合および噴霧乾燥によって得られたNa3Zr2Si2PO12粒子 方法。図 2(a) は、加工後の Na3Zr2Si2PO12 粒子の SEM 写真です。 従来の混合。写真からも形状がわかると思いますが、 粒子は不規則で、一部の粒子の直径は 20 μm に達します。 従来の混合後の粒子のサイズが大きく、 形が不ぞろい。図2(b~c)はNa3Zr2Si2PO12粒子のSEM写真を示しています。 スプレー乾燥後。粒子は球状であり、粒子径は 5 μm 未満、粒子の形状が規則的であり、粒子であることを示します。 噴霧乾燥後はサイズ分布がより集中します。図 2(d) は TEM です。 噴霧乾燥後のNa3Zr2Si2PO12粒子の表面の写真。の 粒子の表面は、厚さの結合剤の層で均一にコーティングされています。 これはセラミック粒子間の接触をより密にするのに役立ちます。

図2 従来のNa3Zr2Si2PO12粒子のSEM画像 混合(a)と噴霧乾燥(b〜c)、および噴霧後のNa3Zr2Si2PO12粒子表面のTEM画像(d) 乾燥
図 3 に粒子サイズを示します ポリビニルアルコールでコーティングされたNa3Zr2Si2PO12(NZSP)の分布図 従来の混合とポリビニルアルコールでコーティングされたNa3Zr2Si2PO12によって得られます。 スプレードライ法により得られる(SD-NZSP)。ことがわかります。 SD-NZSP粒度分布曲線の半値幅が狭い NZSP の粒子サイズ曲線よりも大きく、粒子サイズが 噴霧乾燥後の分布はより濃縮されます。これは基本的には これは、図 2(a、b) の SEM 写真に示された結果と一致しています。で さらに、噴霧乾燥後の粒度分布曲線は、 正規分布。この粒子サイズのグラデーションにより、効果的に粒子径を増加させることができます。 粒子間の接触が起こり、グリーンボディの気孔率が減少します。示されているように 表 2 では、 従来の混合方法では 83.01%、Na3Zr2Si2PO12 の密度は 噴霧乾燥法で製造されたグリーンボディは 89.12% に増加します。順番に Na3Zr2Si2PO12 粒子サイズがセラミック密度に及ぼす影響をさらに調査する 導電率、断面スキャン、密度測定、 導電性試験は、次のようにして得られたNa3Zr2Si2PO12セラミックシートに対して実施されました。 従来の混合および噴霧乾燥方法。
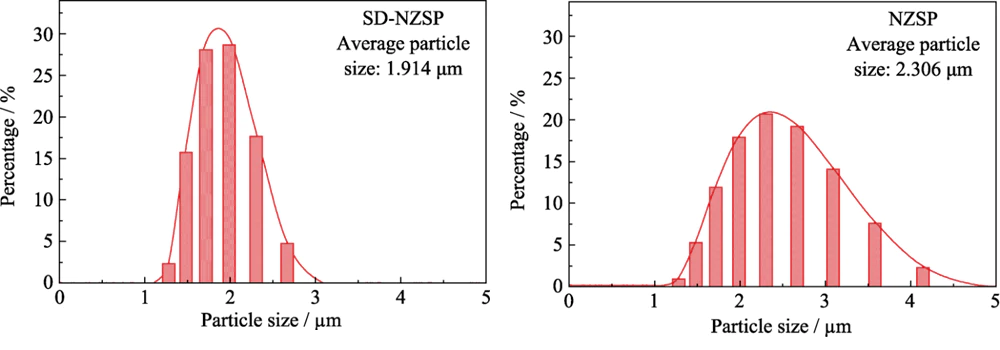
図。 3 Na3Zr2Si2PO12 粒子サイズ 従来の混合 (NZSP) および噴霧乾燥 (SD-NZSP) のプロファイルを測定 レーザー粒子分析装置による
表 2 焼結パラメータと密度測定パラメータ Na3Zr2Si2PO12固体電解質の測定結果と グリーンボディおよびセラミックシート
|
サンプル |
プロセス温度/â |
時間/時間 |
m/g |
エタノール/(g・cm-3) |
水没/g |
現実/(g·cm-3) |
理論値/(g·cm-3) |
相対/% |
|
GB |
- |
- |
0.2902 |
0.785 |
0.2056 |
2.693 |
3.244 |
83.01 |
|
SD-GB |
- |
- |
0.2880 |
0.785 |
0.2098 |
2.891 |
3.244 |
89.12 |
|
CS-NZSP |
1250 |
6 |
0.2672 |
0.785 |
0.1938 |
2.858 |
3.244 |
88.10 |
|
SD-CS-NZSP |
1250 |
6 |
0.2644 |
0.785 |
0.1988 |
3.164 |
3.244 |
97.53 |
図 4 は、 Na3Zr2Si2PO12セラミックシート、その断面形態と元素 分析図。図 4(a) に、その断面形態を示します。 従来の焼結法により得られたセラミックス片。観察されました セラミックシートの断面には不規則な細孔が多数存在しており、 局所的な細孔直径は 5 μm を超えました。その理由は、粒子の大きさにあります。 粉砕後は不均一で、粒子が大きく、緻密ではありません。 粒子間の接触により、セラミック内のより不規則な細孔が生成されます。 二次焼結工程中のシート。図 4(b) は、 噴霧乾燥により得られたセラミック片の断面形態 方法。結晶粒同士が密接しており、 目立った毛穴はありません。これは、Na3Zr2Si2PO12 粒子が規則的な形状をしていることを示しています。 粒度分布が濃縮されており、容易に高密度が得られます。 二次焼結プロセス中のセラミックシート。密度の増加 後のセラミック本体の収縮の増加にも反映されています。 図 4(c) に示すように、焼結します。左側は、次の方法で得られたセラミック片です。 従来の焼結法、直径11.34mm、収縮率 割合はわずか5.5%。右側は噴霧乾燥によって得られたセラミック片です。 直径10.36mm、収縮率13.7%。するために サンプル中の各元素の組成を調査し、元素分析を行いました。 セラミック片の断面に対して実行されます (図 4(b))。 4(d~g)が得られました。各元素の含有量を表3に示す。 元素はセラミック片の断面に均一に分布しており、 要素の集約はありません。表 3 によれば、 Na と P の原子百分率は 2.98:1 であり、これは基本的に 標準化学式は Na:P=3:1 で、過剰な Na と P が体内に存在することを示しています。 原材料は、製造中の Na と P の揮発を補うことができます。 焼結プロセス

図。 4 CS-NZSP (a) および CS-NZSP のスライス切片の SEM 画像 SD-CS-NZSP (b)、対応する写真 (c) および元素マッピング画像 (d-g) SD-CS-NZSP
表 3 スプレーによる Na3Zr2Si2PO12 セラミックスライス切片の元素分析 乾燥/%
|
要素 |
OK |
ナ・K |
Si K |
PK |
ZrL |
|
原子百分率 |
60.10 |
15.09 |
9.94 |
5.06 |
9.81 |
|
重量パーセント |
36.43 |
13.13 |
10.59 |
5.94 |
33.91 |
2.2 Na3Zr2Si2PO12 セラミックシートの密度
実験では次の密度を測定しました。 アルキメデスの方法による Na3Zr2Si2PO12 セラミック シート [30]。勉強するために Na3Zr2Si2PO12セラミックの密度に対する造粒法の影響 シート、セラミックシート調製の実験パラメータでは、 実験パラメータ(焼結温度、保持時間など) 対照実験群は造粒方法以外は同じに保った。で 実験による測定誤差が密度に及ぼす影響を軽減するため 結果として、セラミックシートサンプルに対して密度測定を繰り返しました。 実験における各調製方法で得られたもの。実験から 表 4 に示すデータから、CS-NZSP セラミックの密度が 従来の焼結法で得られるシートは88.1%であり、基本的には これは文献[21]で報告された結果と一致しています。の密度 噴霧乾燥によって得られたSD-CS-NZSPセラミックシートは97.5%に達します。 従来の焼結法で現在達成されている最高値 元素ドーピング。 Na3Zr2Si2PO12セラミックの密度よりもさらに高い 文献で報告されている他の焼結方法によって得られたシート。のような マイクロ波焼結法 (96%) [23]、冷間焼結法 (93%) [24]、液体 相焼結法 (93%) [26] および放電プラズマ焼結法 (97.0%) [29].
表 4 CS-NZSP および CS-NZSP のイオン伝導度 SD-CS-NZSP 室温
|
サンプル |
sb/(SÂ・cm-1) |
sgb/(S·cm-1) |
st/(S·cm-1) |
Ea/eV |
|
CS-NZSP |
1.28×10-3 |
8.03×10-4 |
4.94×10-4 |
0.34 |
|
SD-CS-NZSP |
1.64×10-3 |
1.21×10-3 |
6.96×10-4 |
0.32 |
2.3 Na3Zr2Si2PO12 の電気的性能 テスト
図5(a)は室温を示しています。 セラミックウェーハの電気化学インピーダンススペクトル (EIS) により得られます。 従来の焼結法と噴霧乾燥法。の半円は、 図は粒界の並列インピーダンス特性を反映しています インピーダンスと容量性リアクタンス。の左側との交差点 半円と横軸は粒子の抵抗を表します。の 横軸の半円の幅は粒子の抵抗を反映します。 半円の後の斜線はインピーダンスを表します。 ブロッキング電極/電解質界面の特性[36]。による 図 4 の EIS をフィッティングすると、CS-NZSP および SD-CS-NZSP のイオン伝導率が得られます。 を得ることができます。実験データを表 4 に示します。 噴霧乾燥により得られたSD-CS-NZSPの温度イオン伝導度 法は 6.96 × 10-4 Sâcm-1 であり、 CS-NZSPのそれ(4.94×10-4) S∈cm-1)は従来の焼結法で得られます。を通じて EIS フィッティングのデータ分析では、SD-CS-NZSP の方が高いことがわかります。 密度は粒界抵抗が小さく、室温が高いイオン性 導電率。
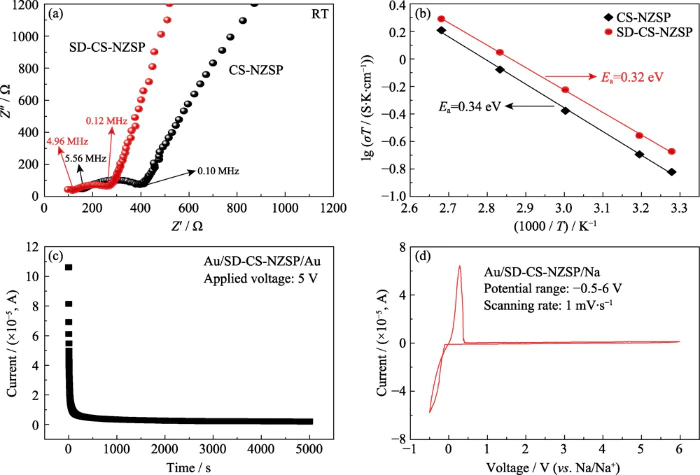
図5 (a) 室温での EIS スペクトルおよび (b) CS-NZSP および SD-CS-NZSP のアレニウス プロット。 (c) DC 定電位分極 SD-CS-NZSP の電流および (d) 電気化学ウィンドウ
図 5(b) は、次のアレニウス曲線を示しています。 異なる調製方法で得られたセラミックシートの場合は室温~100℃ 方法。図からわかるように、導電率は次のように増加します。 気温の上昇。温度が100℃に達すると、導電率は SD-CS-NZSP の強度は 5.24×10-3 Sâcm-1 に達します。これは次数です。 室温の導電率よりも大きい。その活性化エネルギー アレニウスの式 Ï=Aexp(-Ea/kT) [7] に従って当てはめられます。の活性化エネルギーは、 CS-NZSP と SD-CS-NZSP はそれぞれ 0.34 eV と 0.32 eV と得られました。 は YANG らの報告に似ています。 [18].
固体電解質材料が持つべきもの 高いイオン伝導性と低い電子伝導性の両方。したがって、 SD-CS-NZSPの電子伝導度を直流で測定しました 分極 (DC)、対応する分極曲線を図に示します。 5(c)。図からわかるように、テスト時間が長くなると、 分極電流は徐々に減少します。テスト時間が 5000 秒に達すると、 分極電流 (I=3.1 μA) はテスト時間とともに変化しなくなりました。 長引く。式(2、3)で計算すると、 SD-CS-NZSP は 1.23 × 10-7 S · cm-1 であり、ナトリウムイオン 移行数は 0.9998 です。この研究では電気化学ウィンドウも測定されました サイクリックボルタンメトリー (CV) による SD-CS-NZSP の解析 [18]。図 5(d) に示すように、2 つの 酸化と還元のピークは 0 V 付近に現れ、ストリッピングを表します。 およびナトリウムの沈着はそれぞれ[20]。これ以外に酸化還元はありません スキャンされた電圧範囲内でピークが観察されました。ということは、 電圧中の電解液の分解による電流の変化がない これは、SD-CS-NZSP が良好な電気化学的安定性を持っていることを示しています。 広い電気化学ウィンドウ (6 V (対 Na/Na+)) はナトリウムイオンに適合します。 固体電解質から高電圧陰極材料など ニッケルマンガンベースの正極材料は、 ナトリウムイオン電池のエネルギー密度
3 結論
高温固相法は、 焼結温度で純相Na3Zr2Si2PO12粉末を合成するために使用される 前駆体に過剰な Na と P を導入することにより、1150 °C の温度に達します。スプレードライを使用する 粉末を球状に造粒するため、ポリビニルアルコールバインダーが均一に分散されます。 Na3Zr2Si2PO12粒子の表面被覆量と粒子径 分布は正規分布に近いです。準備されたものの密度 Na3Zr2Si2PO12セラミックは97.5%に達します。密度の増加により効果的に削減が可能 粒界抵抗が大きく、イオン伝導率は室温で6.96×10-4 S・cm-1に達し、セラミックシートよりも高い 従来の焼結法(4.94×10-4 S×cm-1)で製造。さらに、 噴霧乾燥法で製造されたセラミックは広い電気化学窓を持っています (6 V (対 Na/Na+)) で、高電圧カソード材料と適合させることができます。 バッテリーのエネルギー密度を高めます。スプレーしているのがわかります 乾燥法はNa3Zr2Si2PO12セラミック電解質を調製する効果的な方法です 高密度でイオン伝導性が高く、他のタイプにも適しています セラミック固体電解質
参考文献
[1] JIAN Z L、ZHAO L、PAN H L、他。 ナトリウムイオン電池用の新しい電極材料としてカーボンコーティングされたNa3V2(PO4)3。 電気化学コミュニケーションズ、2012、14(1):86-89.
[2] ZHAO L、ZHAO JM、HU Y S、他。 高性能アノード材料としてのテレフタル酸二ナトリウム (Na2C8H4O4) 低コストの室温ナトリウムイオン電池。先端エネルギー材料、 2012,2(8):962-965.
[3] RUAN Y L、GUO F、LIU J J、他。 Na3Zr2Si2PO12 セラミック電解質と界面の最適化 高性能全固体ナトリウム電池。セラミックスインターナショナル、 2019,45(2):1770-1776.
[4] VETTER J、NOVAK P、WAGNER M R、他。 リチウムイオン電池の劣化メカニズム。ジャーナル・オブ・パワー・ソース、 2005,147(1/2):269-281.
[5] 鎌谷 信、本間 和、山川 裕、他。あ リチウム超イオン伝導体。ネイチャー マテリアルズ、2011、10(9):682-686.
[6] TARASCON JM、ARMAND M. 問題と 充電式リチウム電池が直面する課題。自然、 2001,414(6861):359-367.
[7] KHOKHAR WA、ZHAO N、HUANG WL、他。 Na および Li 固体電解質における金属浸透の異なる挙動。 ACS アプライド マテリアルズ & インターフェイス、12(48):53781-53787.
[8] オーデンホーフェン J F M、バジェット L、ノッテン P H L. 全固体リチウムイオンマイクロ電池: さまざまな 3 つの電池のレビュー 次元の概念。先端エネルギー材料、2011、1(1):10-33.
[9] ZHAO C L、LIU L L、QI X G、他。 全固体ナトリウム電池。先端エネルギー材料、2017、8(17):1703012.
[10] 林 亜、野井 和、作田 亜、他。 室温再充電可能なナトリウム用の超イオン性ガラスセラミック電解質 電池。 Nature Communications、2012、3:856.
[11] LOU S F、ZHANG F、FU C K、他。 全固体電池における界面の問題と課題: リチウム、ナトリウム、 そしてその先へ。アドバンストマテリアルズ、2020、33(6):2000721.
[12] HUANG W L、ZHAO N、BIZ J、他。できる ガーネット固体電解質による Li の浸透を排除する解決策は見つかりますか? Materials Today Nano、2020、10:100075.
[13] JIAN Z L、HU Y S、JI X L、他。 エネルギー貯蔵用の NASICON 構造材料。先端材料、 2016,29(20):1601925.
[14] HOU W R、GUO X W、SHEN X Y、他。 全固体ナトリウム電池の固体電解質と界面:進歩 そして視点。ナノエネルギー、2018、52:279-291.
[15] グッドイナフ J B、ホン ハイ P、カファラス J A. 骨格構造における Na+ イオンの高速輸送。材料研究紀要、 1976,11(2):203-220.
[16] HONG HYP. 結晶構造と Na1+xZr2SixP3-xO12系における結晶化学。材料研究 紀要、1976 年、11(2):173-182.
[17] RAN L B、BAKTASH A、LI M、他。 Sc、 Ge を同時ドーピングした NASICON は、全固体ナトリウム イオン電池の性能を向上させます。 エネルギー貯蔵材料、2021、40:282-291.
[18] YANG J、LIU G Z、AVDEEV M、他。 超安定な全固体ナトリウム二次電池。 ACSエネルギーレター、 2020,5(9):2835-2841.
[19] LENG HY、HUANG JJ、NIE JY、他。 Na3.256Mg0.128Zr1.872Si2PO12固体の冷間焼結とイオン伝導率 電解質。ジャーナル オブ パワー ソース、2018、391:170-179.
[20] HUANG C C、YANG G M、YU W H、他。 ガリウム置換Nasicon Na3Zr2Si2PO12固体電解質。合金ジャーナル And Compounds、2021、855:157501.
[21] ZHANG ZZ、ZHANG Q H、SHI JN、他。 全固体ナトリウム電池用の自己形成型複合電解質。 超長サイクル寿命。先端エネルギー材料、2017、7(4):1601196.
[22] アナンタラムル N、RAO K K、ランバブ G、 他。ナシコン系素材を幅広くレビュー。材料ジャーナル サイエンス、2011、46(9):2821-2837.
[23] WANG X X、LIU Z H、TANG Y H 他 Na3Zr2Si2PO12固体の低温急速マイクロ波焼結 Naイオン電池用電解液。ジャーナル オブ パワー ソース、2021、481:228924.
年[24] GRADY Z M、TSUJI K、NDAYISHIMIYE A、他 アル。 400 µm 以下での固体 NASICON ナトリウムイオン電解質の高密度化 溶融水酸化物溶媒を使用した冷間焼結による。 ACS応用エネルギー材料、 2020,3(5):4356-4366.
[25] SHAO Y J、ZHONG G M、LU Y X 他。あ Naイオンを強化した新しいNASICONベースのガラスセラミック複合電解質 導電性。エネルギー貯蔵材料、2019、23:514-521.
年[26] LENG HY、NIE JY、LUO J. 組み合わせ 冷間焼結およびBi2O3活性化液相焼結による製造 低温での高導電性MgドープNASICON。ジャーナル マテリオミクス、2019、5(2):237-246. 年
年[27] OH JAS、HELC、PLEWA A、他。 Na+ を強化した複合 NASICON (Na3Zr2Si2PO12) 固体電解質 イオン伝導率: 液相焼結の効果。 ACS アプライド マテリアルズ & インターフェース、2019、11(43):40125-40133. 年
年[28] ダ・シルバ・J・GP、ブラム・M、ラプテフ・アム、他 アル。ナトリウムベースの NASICON 電解質の焼結: 比較研究 冷間焼結法、フィールドアシスト焼結法、および従来の焼結法の間。のジャーナル 欧州セラミック協会、2019、39(8):2697-2702.
年[29] WANG H、OKUBO K、INADA M、他。低い Na2O-Nb2O5-P2O5 ガラスにより促進される温度密度の高い NASICON ベースのセラミックス 添加剤および放電プラズマ焼結。ソリッド ステート イオニクス、2018、322:54-60.
[30] HUO HY、GAO J、ZHAO N、他。あ デンドライトフリーの固体リチウム用の柔軟な電子ブロッキング界面シールド 金属電池。 Nature Communications、2021、12(1):176.
[31] JIA MY、ZHAO N、HUO HY 他。 ガーネット電解質の総合的研究 応用志向の固体リチウム電池。電気化学エネルギーのレビュー、 2020,3(4):656-689. 年
[32] ZHAO N、KHOKHAR W、BI Z J、他。 固体ガーネット電池。ジュール、2019、3(5):1190-1199.
[33] ヴァートゥルーエン B、エスラギ N、ピフェット C、他 アル。リチウムイオン電池およびナトリウムイオン電池の電極材料の噴霧乾燥。 資料、2018,11(7):1076.
年[34] KOU ZY、MIAO C、WANG ZY 他。 新しい NASICON 型構造 Li1.3Al0.3Ti1.7SixP5(3-0.8x)O12 固体 リチウムイオン電池用のイオン伝導率が向上した電解質。固体 ステート アイオニクス、2019、343:115090.
[35] SHEN L、YANG J、LIU G Z、他。高い イオン伝導性とデンドライト耐性を備えたNASICON固体電解質 全固体ナトリウム電池。 Materials Today Energy、2021、20:100691.
[36] LI Y Q、WANG Z、LIC L、他。 リチウムガーネット固体の緻密化とイオン伝導の向上 流動酸素焼結による電解質の生成。ジャーナル・オブ・パワー・ソース、 2014,248:642-646.



